Решение задачи по хими на определение формулы гексеновой кислоты
Задача 1.41.
Массовая доля водорода в некоторой одноосновной карбоновой кислоте составляет 8,77%, а в сложном эфире, образованном этой кислотой с этанолом, — 9,86% . Определите молекулярную формулу кислоты.
Дано:
массовая доля водорода в кислоте: 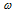 (Н) = 8,77%;
(Н) = 8,77%;
массовая доля водорода в эфире: 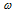 (Н) = 9,86%.
(Н) = 9,86%.
Найти: молекулярную формулу кислоты.
Решение:
Шаг 1. В состав обоих соединений входит углерод, водород и кислород. Отсутствие информации о насыщенности углеводородного радикала в карбоновой кислоте не позволяет выявить соотношение индексов у углерода и водорода. Поэтому формула искомой кислоты будет содержать две неизвестные величины: СхНуСООН. При решении данной задачи удобнее использовать формулу с указанием функциональной карбоксильной группы, так как с ее участием образуется сложный эфир с этанолом. Формула этанола нам известна, и поэтому мы легко можем записать получающийся эфир:
СхНуСОО—С2Н5.
В нем присутствуют те же неизвестные х и у.
Шаг 2. В условии нет указаний на химическую реакцию.
Шаг 3. Соотношение атомов по обычному алгоритму с использованием данных из условия определить не удастся. Это обстоятельство не дает возможности найти и . Поэтому мы сразу переходим к 5 шагу алгоритма.
Шаг 5. Выявление возможно лишь по встречному алгоритму с составлением системы из двух математических уравнений. Каждое из них легко получить на основе соотношения для вычисления массовой доли, как мы это делали в предыдущей задаче. Для кислоты и эфира составляется свое уравнение по массовой доле водорода.
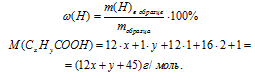
Масса 1 моль СХНУСООН составляет (12х + у + 45) г, и вклад водорода в эту массу будет (1 . у + 1 ) г. Подставляем значение масс выбранного образца и водорода в нем в соотношение для вычисления массовой доли:
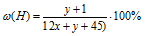
Приравнивая это выражение к значению массовой доли водорода в кислоте из условия, получаем первое математическое уравнение:
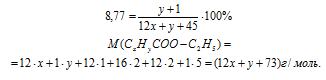
Масса 1 моль СхНуСОО—С2Н5 составляет (12х + у + 73) г, и вклад водорода в эту массу будет (1 . у + 5) г. Подставляем значение масс выбранного образца и водорода в нем в соотношение для вычисления массовой доли:
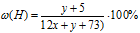
Приравнивая это выражение к значению массовой доли водорода в эфире из условия, получаем второе математическое уравнение:
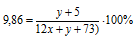
Объединяем полученные математические уравнения в систему:
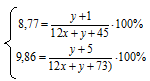
В результате ее решения получаем: х = 5; у = 9.
Подставляем эти значения в формулу карбоновой кислоты: С5Н9СООН.
Ответ: С5Н9СООН.

