Решение задач по теме "Классы неорганических соединений"
Задача 149.
Можно ли получить раствор, содержащий одновременно: а) Ва(ОН)2 и HCl; б) СаСI2 и Na2СО3; в) NaCl и AgNO3 ; г) КСI и NaNO3. Указать, какие комбинации невозможны и почему.
Решение:
а) Ba(OH)2 и HCl – , поэтому в водных растворах диссоциируют полностью:
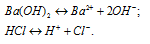
Находящиеся в растворе ионы Ba2+ и Cl– не связываются с ионами H+ и OH– с образованием осадка, газа или . Поэтому раствор Ba(OH)2 и HCl будет существовать.
б) Растворимые соли CaCl2 и Na2CO3 как в водных растворах диссоциируют полностью по схемам:
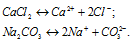
Ионы Ca2+ и CO3– связываются друг с другом, образуя осадок - не растворимая соль. В растворе останутся ионы Cl– и OH–, которые не связываются друг с другом, молекулами CaCO3 и ионами воды H+ и OH-. Поэтому невозможно получить раствор, содержащий одновременно CaCl2 и Na2CO3, так как выпадает осадок СаСО3.
в) NaCl и AgNO3, как в водных растворах диссоциируют полностью по схемам:
NaCl ⇔ Na+ + Cl-;
AgNO3 ⇔ Ag+ + NO3-.
Ионы Ag+ и Cl- связываются друг с другом, образуя осадок AgCl. В растворе остаются ионы Na+ и NO3-, которые не связываются друг с другом с молекулами AgCl, ионами воды H+ и OH- и не образуют осадок, газ или слабый электролит. Поэтому невозможно получить раствор, содержащий одновременно NaCl и AgNO3, так как выпадает осадок AgCl.
г) КСI и NaNO3 – растворимые соли, которые в водных растворах полностью распадаются на ионы:
KCl ⇔ K+ + Cl-;
NaNO3 ⇔ Na+ + NO3-.
Образовавшиеся ионы K+, Na+, Cl- и NO3- не связываются друг с другом и ионами воды H+ и OH- и не образуют осадок, газ или слабодиссоциируемое вещество. Таким образом, можно получить раствор одновременно содержащий КСI и NaNO3.
Задача 150.
Какие из перечисленных кислот образуют кислые соли: HJ, H2Se, H2SeO3, H2C2O4, CH3COOH.
Решение:
образуют многоосновные кислоты, в которых атомы водорода не все замещены на катионы кислоты. Так как кислоты HJ и CH3COOH содержат по одному катиону водорода в составе молекул, то они не могут образовать кислых солей. Кислоты H2Se, H2SeO3, H2C2O4 являются , то они могут образовать кислые соли при замещении одного атома водорода на катион металла. При взаимодействии этих кислот с основаниями, в случае, если кислота взята в избытке, образуется , например:
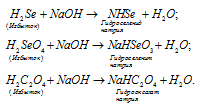
Названия образуются, так же как и средних, но при этом добавляют приставку «гидро» и указывают наличие незамещённых атомов водорода, число которых обозначают греческими числительными («ди», «три» и т.д.). Например: NaH2HO4 - дигидроортофосфат натрия; KH2AsO4 – дигидроортоарсенат калия; Mg(HCO3)2 – гидрокарбонат магния.
Задача 151.
Какие кислоты могут быть получены непосредственным взаимодействием с водой оксидов: Р2О5, СО2, N2O5, NO2, SO2?
Решение:
а) При взаимодействии P2O5 с водой могут образоваться различные , например метафосфорная HPO3 и ортофосфорная H3PO4:
Р2О5 + H2O → 2HPO3;
Р2О5 + 3H2O → 2H3PO4.
б) При пропускании углекислого газа через воду образуется раствор слабой угольной кислоты H2CO3:
CO2 + H2O → H2CO3
в) При растворении N2O5 в воде образуется азотная кислота HNO3 – .
г) при взаимодействии NO2 с водой может быть получена смесь двух кислот азотистой HNO2 и азотной HNO3:
2NO2 + H2O → HNO2 + HNO3
В присутствии избытка кислорода в воде образуется только :
4NO2 + O2 + 2H2O → 4HNO3
д) SO2 хорошо растворим в воде (36 об. ч. SO2 на 1 об. ч. Н2О при 20 0С), при этом образуется сернистая кислота H2SO3 – кислота средней силы:
SO2 + H2O → H2SO3.
Задача 152.
С какими из перечисленных ниже веществ будет реагировать соляная кислота: N2O5, Zn(ОН)2, СаО, AgNO3, Н3РO3, Н2SO4? Составить уравнения реакций.
Решение:
а) Оксид азота (V) N2O5 является кислотным оксидом, поэтому не реагирует с соляной кислотой HCl.
б) гидроксид цинка Zn(ОН)2 является , поэтому реагирует как с основаниями, так и с кислотами. Реакция между Zn(ОН)2 и HCl протекает:
Zn(ОН)2 + 2HCl →ZnCl2 + 2H2O
в) Оксид кальция СаО является основным оксидом, поэтому реагирует с соляной кислотой:
CaO + 2HCl → CaCl2 + H2O
г) Нитрат серебра AgNO3 – сильный электролит, который в водных растворах диссоциирует на ионы Ag+ и NO3-, а соляная кислота как электролит распадается на ионы H+ и Cl-. Ионы Ag+ и Cl-, соединяясь, образуют нерастворимую соль AgCl, которая выпадает в осадок. Реакция между нитратом серебра и соляной кислотой протекает по схеме:
AgNO3 + HCl →AgC↓ + HNO3
д) Ортофосфорная кислота Н3РO4, серная кислота H2SO4 и соляная кислота HCl – электролиты, которые в водных растворах распадаются на ионы:
Н3Р04 ⇔ 3H+ + PO43-;
H2SO4⇔ 2H+ + SO42-;
HCl ⇔ H+ + Cl-.
Ионы PO43-, SO42-, H+ и Cl- не связываются друг с другом, не образуют осадок, газ или малодиссоциируемое вещество. Поэтому Н3РO3 и Н2SO4 не реагируют с HCl.
Задача 153.
Какие из указанных веществ реагируют с гидроксидом натрия: HNO3, CaO, CO2, CuSO4, Cd(OH)2, P2O5. Составить уравнения реакций.
Решение:
а) как кислота вступает в реакцию нейтрализации с основанием NaOH, при этом образуется соль и вода:
HNO3 + NaOH → NaNO3 + H2O
б) Оксид кальция СаО – основной оксид, поэтому не будет реагировать с NaOH – сильным основанием.
в) Оксид углерода (II) СО2 – кислотный оксид, поэтому будет реагировать с гидроксидом NaOH с образованием соли и воды:
CO2 + 2NaOH → NaO3 + H2O
г) CuSO4 и NaOH – , поэтому в водных растворах распадаются на ионы:
CuSO4 ⇔ Cu2+ + SO42-;
NaOH ⇔ Na+ + OH-
Ионы Cu2+ и OH- связываются друг с другом, образуя осадок из нерастворимого Cu(OH)2. Значит, между CuSO4 и NaOH реакция протекает по уравнению:
д) Гидроксид кадмия Сd(OH)2 имеет слабо выраженные кислотные свойства, поэтому в растворе гидроксида натрия высокой концентрации при длительном кипячении образует неустойчивые гексагидроксокадмиат(I) – ионы [Cd(OH)6]4-:
Сd(OH)2 + 4NaOH → Na4[Cd(OH)6]
Оксид фосфора(V) Р2О5 – кислотный оксид, поэтому будет реагировать с раствором гидроксида натрия с образованием соли и воды:
Р2О5 + 6NaOH → 2Na3PO4
Задача 154.
Написать уравнения реакций, свидетельствующих об основных свойствах FeO, Cs2O, HgO, Bi2O3.
Решение:
Оксиды FeO, Cs2O, HgO, Bi2O3 имеют основной характер, поэтому все они растворяются в кислотах с образованием соли и воды:
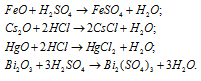
Задача 155.
Написать уравнения реакций, доказывающих кислотный характер SеО2, SО3, Мn2O7, Р2O5, СrО3.
Решение:
Кислотные оксиды SеО2, SО3, Мn2O7, Р2O5 и СrО3 при взаимодействии с водой образуют соответствующие кислоты. Все они проявляют кислотные свойства, взаимодействуют как с основаниями, так и с основными оксидами:
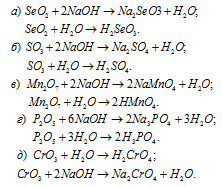
Задача 156.
Составить уравнения реакций получения хлорида магния: а) действием кислоты на металл; б) действием кислоты на основание; в) действием кислоты на соль.
Решение:
Уравнения реакций получения хлорида магния:
а) Действием кислоты на металл:
Ma + 2HCl → MaCl2 + H2↑
б) Действием кислоты на основание:
Mg(OH)2 + 2HCl → MgCl2 + 2H2O
в) Действием кислоты на соль:
MgSO4 + 2HCl → MgCl2 + H2SO4
Задача 157.
Составить уравнения реакций между кислотами и основаниями, приводящих к образованию солей: NaNO3, NaHSO4, Na2HPO4, K2S, Fe2(SO4)3.
Решение:
Уравнения реакций образования солей:
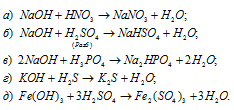
Задача 158.
Какие вещества могут быть получены при взаимодействии кислоты с солью? Кислоты с основанием? Соли с солью? Привести примеры реакций.
Решение:
а) При взаимодействии кислоты с солью могут быть получены кислота и соль, а также и другие вещества, например оксиды и вода:
CuS + 10HNO3 → Cu(NO3)2 + H2SO4 + 8NO2↑ + 4H2O
CaF2 + H2SO4 → CaSO4 + 2HF
б) При взаимодействии кислоты с основанием (реакция нейтрализации) образуются соль и вода:
NaOH + HCl → NaCl + H2O;
Zn(OH)2 + H2SO4 → ZnSO4 + 2H2O
в) Реакция между солями идёт, если при этом образуется малорастворимое соединение (реакция обмена). При взаимодействии соли с солью образуются новые соли, одна из них нерастворима:
AgNO3 + HCl → AgCl↓ + HNO3;
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl

