Описание электронного строения молекул с позиций методов валентных связей и молекулярных орбиталей
Задача 241.
Описать электронное строение молекул СО и СN с позиций методов ВС и МО. Какая из молекул характеризуется большей кратностью связи?
Решение:
а) Электронное строение молекул CO и CN с позиции метода ВС
углерода 1s22s22p2, атома кислорода 1s22s22p4, атома азота 1s22s22p3. Электронное строение их валентных орбиталей в невозбуждённом состоянии может быть представлено следующими графическими схемами:
а) атом углерода:
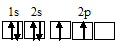
б) атом азота:
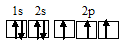
При возбуждении атом углерода переходит в состояние 1s22s12p3, а электронное строение его соответствует схеме:
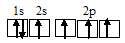
Два неспаренных электрона невозбуждённого атома углерода могут участвовать в образовании двух по обычному механизму с атомом кислорода, имеющем два неспаренных электрона, с образованием молекулы СО. При образовании молекулы CN образуются две по обычному механизму за счёт двух неспаренных электрона атома углерода и двух неспаренных электронов атома азота. CO и CN:
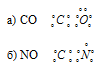
б) Электронное строение молекул CO и CN с позиции метода МО
а) CO и б) CN:
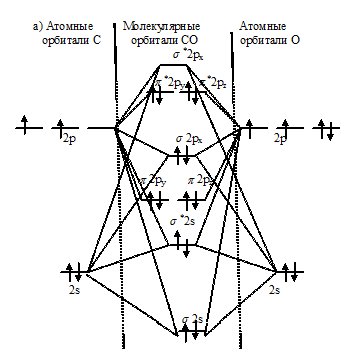
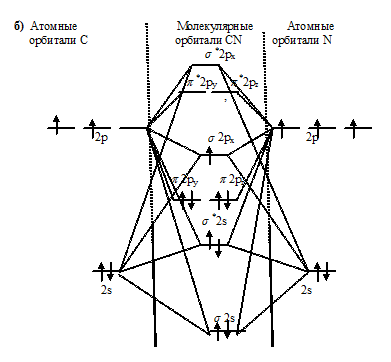
Из приведённых схем следует, что кратность связи в молекуле СО равна 3 [(6 - 0)/2 = 3], а в молекуле NO – 2,5[(5 – 0)/2 = 2,5]. Следовательно, молекула СО по отношению к молекуле NO характеризуется большей устойчивостью, чем больше кратность связи, тем короче связь. Молекула СN имеет один неспаренный электрон на связывающей орбитали, следовательно, она . Молекула СО не имеет неспаренных электронов на связывающих и разрыхляющих орбиталях, значит, она .
Задача 242.
Рассмотреть с позиций метода МО возможность образования молекул В2, F2, BF. Какая из этих молекул наиболее устойчива?
Решение:
а)В2, б) F2, в) BF:
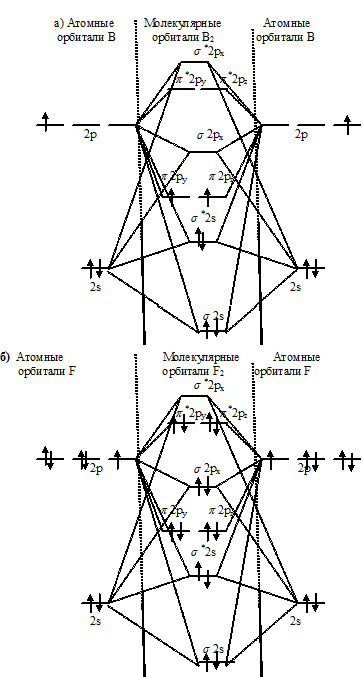
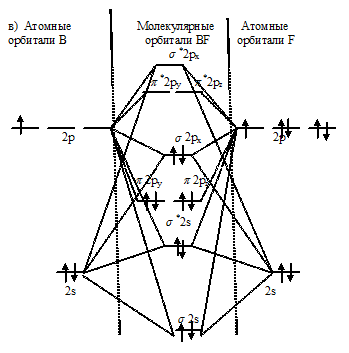
Из составленных В2, F2, BF вытекает, что разность между числом связывающих и разрыхляющих электронов соответственно равны 2, 2 и 6, что отвечает соответственно 1, 1 и 3. Следовательно, молекула BF характеризуется большей между атомами, она должна быть более прочной, чем у В2 и F2.

