Задачи по химии на определение свойств веществ и определение ковалентности атома элемента
Задача 248.
Чему равна ковалентность углерода в молекуле СО: а) двум; б) трем; в) четырем? Потому что: 1) в невозбужденном атоме углерода имеются два неспаренных электрона; 2) атом углерода может быть акцептором электронной пары; 3) в атоме углерода имеются четыре валентных электрона.
Решение:
углерода 1s22s22p2, атома кислорода 1s22s22p4. Электронное строение их валентных орбиталей в невозбуждённом состоянии может быть представлено следующими графическими схемами:
а) атома углерода:
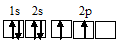
б) атома кислорода:
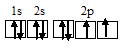
Два не спаренных электрона невозбуждённого атома углерода могут участвовать образовании двух по обычному механизму с атомом кислорода, имеющем два неспаренных электрона, с образованием молекулы СО.
В соединении СО у атома углерода остаётся свободная 2р-орбиталь, которая может быть акцептором электронной пары.
Таким образом, углерода в молекуле СО равна 3 (две за счёт двух неспаренных 2р-электронов и одной свободной 2р-орбитали).
Ответ: б)2.
Задача 249.
Может ли произойти реакция между HF и SiF4: а) может; б) не может?
Потому что: 1) молекула HF полярна, а молекула SiF4 неполярна; 2) обе молекулы не имеют неспаренных электронов; 3) число валентных орбиталей кремния больше четырех и часть их не заселена валентными электронами; 4) число валентных электронов кремния равно четырем; 5) молекула HF может выступать в качестве донора электронной пары.
Решение:
фтора и кремния соответственно 1s22s22p5 и 1s22s22p63s23p23d0.
Электронное строение их валентных орбиталей в невозбуждённом состоянии может быть представлено следующими графическими схемами:
а) атома фтора:
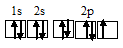
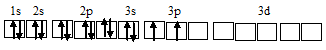
При возбуждении атом кремния переходит в состояние 1s22s22p63s13p3, электронное строение его соответствует схеме:
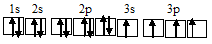
Один неспаренный электрон атома фтора может участвовать в образовании ковалентной связи по обычному механизму с атомом водорода (1s1), имеющим один неспаренный электрон с образованием HF.
Четыре неспаренных электрона возбуждённого атома кремния могут участвовать в образовании четырёх по обычному механизму с атомами водорода (1s1), имеющими по одному неспаренному электрону с образованием SiF4.
Реакция между молекулами HF и SiF4 может произойти, так как в молекуле HF атом фтора имеет три свободные электронные пары (одна на 2s- и две на 2р-орбитали), т.е. молекула HF может выступать в качестве донора электронной пары; в молекуле SiF4 атом кремния имеет пять свободных 3d-орбиталей, т.е. молекула SiF4 может быть .
Ответ: а)3,5.
Задача 250.
Какими магнитными свойствами обладает молекула О2: а) диамагнитна; б) парамагнитна?
Потому что: 1) молекула О2 содержит четное число электронов; 2) суммарный спин молекулы О2 отличен от нуля.
Решение:
О2:
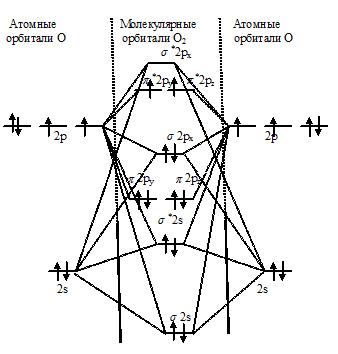
Из вытекает, что на МО молекулы кислорода имеется два неспаренных электрона, которые сообщают молекуле , т. е. суммарный молекулы отличен от нуля (+1).
Ответ: б2.
Задача 251.
Какова кратность связи в молекуле NO: а) два; б) два с половиной; в) три?
Потому что: 1) число связывающих электронов на  - орбиталях равно четырем; 2) число связывающих электронов на пять больше числа разрыхляющих электронов; 3) атом азота имеет три неспаренных электрона.
- орбиталях равно четырем; 2) число связывающих электронов на пять больше числа разрыхляющих электронов; 3) атом азота имеет три неспаренных электрона.
Решение:
NО:
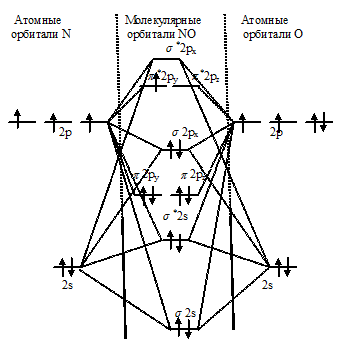
Как видно из схемы в молекуле NO разность между числом связывающих и числом разрыхляющих электронов равна пяти (6 – 1 = 5), что отвечает 2,5 (5/2 = 2,5).
Ответ: б2.

