Соотношение стандартных изменений энтальпии и энтропии реакций
Задача 316.
Для следующих реакций:
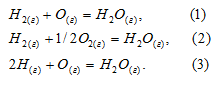
указать правильное соотношение стандартных изменений энтальпии:
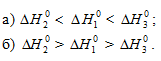
Решение:
По табличным данным образования веществ, участвующих в реакциях равны ( принято считать равными нулю):
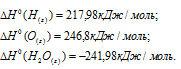
Для расчета 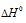 реакций используем уравнение из :
реакций используем уравнение из :
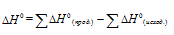
а) Находим реакции:
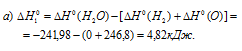
б) Находим реакции:
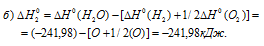
в) Находим :
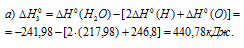
Таким образом, 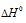 2 и
2 и 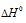 1 <
1 < 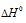 3.
3.
Ответ: а).
Задача 317.
Указать, какие из нижеследующих утверждений правильны для реакций, протекающих в стандартных условиях: а) эндотермические реакции не могут протекать самопроизвольно; б) эндотермические реакции могут протекать при достаточно низких температурах; в) эндотермические реакции могут протекать при достаточно высоких температурах, если изменение энтропии реакции положительно.
Решение:
имеет значение энтальпии 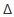 H > 0. Если
H > 0. Если 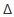 H > 0,
H > 0,  > 0, то в уравнении
> 0, то в уравнении
 =
= 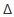 H - T
H - T второй член равенства (- T
второй член равенства (- T ) будет иметь отрицательное значение, поэтому член (
) будет иметь отрицательное значение, поэтому член ( ) примет тоже отрицательное значение только при достаточно большом числовом значении (Т).
) примет тоже отрицательное значение только при достаточно большом числовом значении (Т).
При 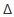 H > 0,
H > 0,  < 0 в уравнении (
< 0 в уравнении ( =
= 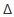 H - T
H - T ) второй член равенства (- T
) второй член равенства (- T ) будет иметь положительное значение, поэтому при любом значении температуры (Т) член (
) будет иметь положительное значение, поэтому при любом значении температуры (Т) член ( ) будет всегда иметь тоже положительное значение. Таким образом, при
) будет всегда иметь тоже положительное значение. Таким образом, при 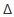 H > 0,
H > 0,  < 0 реакция невозможна при любых значениях температуры; при
< 0 реакция невозможна при любых значениях температуры; при
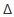 H > 0,
H > 0,  > 0 реакция возможна только при достаточно высоких температурах. Значит, могут протекать при достаточно высоких температурах, если изменение энтропии реакции имеет положительное значение.
> 0 реакция возможна только при достаточно высоких температурах. Значит, могут протекать при достаточно высоких температурах, если изменение энтропии реакции имеет положительное значение.
Ответ: в).
Задача 318.
Не производя вычислений, указать, для каких из перечисленных процессов изменение энтропии положительно:
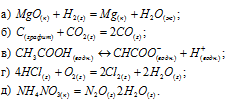
Решение:
а) В реакции не наблюдается изменения общего числа молей веществ, из одного кристаллического и одного газообразного веществ образуется одинаковое число кристаллического и жидкого веществ, это, естественно, приводит к упорядоченности системы, что сопровождается уменьшением энтропии,  < 0.
< 0.
б) В реакции не наблюдается изменения общего числа молей веществ, но число молей газообразных веществ возрастает вдвое, это, естественно, приводит к упорядоченности системы, что сопровождается уменьшением ,  > 0.
> 0.
в) Реакция протекает без изменения агрегатных состояний веществ, но с увеличением молей продуктов реакции, это ведёт к уменьшению упорядоченности системы, значит  > 0.
> 0.
г) В реакции происходит уменьшение, как общего числа молей реагирующих веществ, так и общего числа молей газообразных веществ, это приводит систему в состояние большей упорядоченности, значит  < 0.
< 0.
д) В реакции происходит увеличение общего числа молей реагирующих веществ, и к тому же из кристаллического вещества образуются два газообразных веществ, это приводит к уменьшению упорядоченности системы, значит  > 0.
> 0.
Ответ: б), в), д).
Задача 319.
В каком из следующих случаев реакция возможна при любых температурах: а) 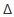 H < 0;
H < 0; > 0; 6)
> 0; 6) 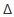 H < 0,
H < 0,  < 0; в)
< 0; в) 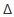 H > 0,
H > 0, >0?
>0?
Решение:
а) При 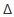 H < 0,
H < 0,  > 0 в уравнении (
> 0 в уравнении ( =
= 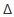 H - T
H - T ) второй член равенства ( - T
) второй член равенства ( - T ) будет иметь отрицательное значение при любых значениях температуры (Т). Значит,
) будет иметь отрицательное значение при любых значениях температуры (Т). Значит,  при
при 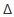 H < 0,
H < 0, > 0 всегда имеет отрицательное значение, поэтому реакция возможна при любых температуре.
> 0 всегда имеет отрицательное значение, поэтому реакция возможна при любых температуре.
б) При 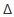 H < 0,
H < 0,  < 0 реакция возможна при условии, что
< 0 реакция возможна при условии, что 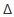 H в уравнении (
H в уравнении ( =
= 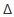 H - T
H - T ) больше по абсолютному значению, чем член (T
) больше по абсолютному значению, чем член (T ); поскольку абсолютное значение члена (T
); поскольку абсолютное значение члена (T ) с ростом множителя (Т) увеличивается, то указанное условие будет осуществляться при достаточно низких температурах, т.е. при низких температурах наиболее вероятно самопроизвольное протекание , даже если при этом уменьшается.
) с ростом множителя (Т) увеличивается, то указанное условие будет осуществляться при достаточно низких температурах, т.е. при низких температурах наиболее вероятно самопроизвольное протекание , даже если при этом уменьшается.
в) При 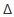 H > 0,
H > 0, > 0 в уравнении (
> 0 в уравнении ( =
= 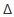 H - T
H - T ) второй член равенства ( - T
) второй член равенства ( - T ) будет иметь отрицательное значение, поэтому член (
) будет иметь отрицательное значение, поэтому член ( ) примет тоже отрицательное значение только при достаточно большом числовом значении (Т). Член (
) примет тоже отрицательное значение только при достаточно большом числовом значении (Т). Член ( ) может быть отрицателен только при очень высоких значениях температуры (Т). Реакция возможна только при достаточно высоких температурах, потому что с ростом члена (Т) будет наблюдаться уменьшение значения члена (
) может быть отрицателен только при очень высоких значениях температуры (Т). Реакция возможна только при достаточно высоких температурах, потому что с ростом члена (Т) будет наблюдаться уменьшение значения члена ( ).
).
Ответ: а).

