Решение задач по химии на расчет нормальности раствора щелочи и кислоты
Задача 443.
На нейтрализацию 40 мл раствора щелочи израсходовано 25 мл 0,5н. раствора H2SO4. Какова нормальность раствора щелочи? Какой объем 0,5 Н. раствора НСI потребовался бы для той же цели?
Решение:
Для вычисления по результатам используем математическое выражение следствия из (так называемое правило пропорциональности):
CЭ(А) . V(A) = CЭ(B) . V(B),
где
CЭ(А) и CЭ(B) - А и В, моль/л; V(A) и V(B) - объёмы растворов веществ А и В.
Тогда

Ответ: 0,3H; 24 мл.
Задача 444.
Для нейтрализации раствора, содержащего 2,25 г кислоты, потребовалось 25 мл 2н. раствора щелочи. Определить эквивалентную массу кислоты.
Решение:
Для расчета используем формулу:
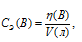 где
где
СЭ(В) – В; V(мл) – объём раствора; n(B) – В.
Тогда
n(щелочи) = СЭ(щелочи) . V(щелочи) = 2 . 0,025 = 0,05Н
Кислота и щёлочь реагируют в , поэтому равно количеству кислоты. Зная и её массу можно вычислить молярную её по формуле:
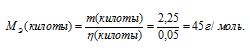
Ответ: 45 г/моль.
Задача 445.
На нейтрализацию 20 мл раствора, содержащего в 1 л 12 г щелочи, израсходовано 24 мл 0,25н. раствора кислоты. Рассчитать эквивалентную массу щелочи.
Решение:
Для расчета используем формулу:
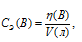 где
где
СЭ(В) – В; V(мл) – объём раствора; n(B) – В.
Тогда
n(кислоты) = СЭ(кислоты) . V(кислоты) = 0,25 . 24 = 0,006Н
Теперь рассчитаем массу щёлочи из пропорции:
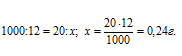
Кислота и щёлочь реагируют в , поэтому равно количеству кислоты. Зная и её массу можно вычислить её по формуле:
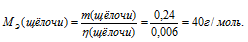
Ответ: 40г/моль.
Задача 446.
Какой объем 15%-ного (по массе) раствора H2SO4 (p = 1,10 г/мл) потребуется для полного растворения 24,3 г Мg, 27 г Al?
Решение:
а) Находим массу 1000 мл раствора по формуле:
m(p-pa) = p . V,
где
p - плотность, а V – объём раствора, получим:
m(p-pa) = 1,10 . 1000 = 1100г.
Массу серной кислоты рассчитаем из пропорции:
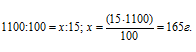
Уравнение реакции имеет вид:
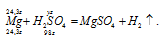
Рассчитаем объём раствора серной кислоты необходимый для растворения 24,3г магния из пропорции
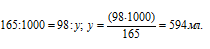
б) Уравнение реакции имеет вид:
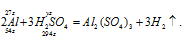
Рассчитаем массу серной кислоты, которая прореагировала с 27г алюминия из пропорции:
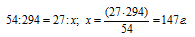
Рассчитаем объём раствора серной кислоты необходимый для растворения 27г алюминия из пропорции:
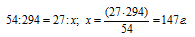
Ответ: 594 мл; 891 мл.

