Магнитные (парамагнитные и диамагнитные) свойства веществ
Задача 934.
Какие из перечисленных молекул парамагнитны: а) NO; б) NO2; в) N2O3; г) N2O4; д) N2O5; е) N2O?
Решение:
Напишите сокращенные формулы молекул методом МО:
а) Молекула NО. На МО молекулы оксида азота (II) должны разместиться 11 электронов: пять азота – 2s22p3 и шесть кислорода – 2s22p4. Размещая их на МО получаем следующую конфигурацию основного состояния:
NО[КК(σsCB)2(σs разр.)2(πyCB)2(πzCB)2(σхCB)2(πy разр.)1]
NO парамагнитна, так как содержит один неспаренный электрон.
б) Молекула NO2. На МО молекулы оксида азота (IV) должны разместиться 17 электронов: пять азота – 2s22p3 и по шесть кислорода – 2s22p4 от двух атомов. Размещая их на МО получаем следующую конфигурацию основного состояния:
NО2 [(ККσs)2(σs)2(σsСВ)2(σzСВ)2(πyCB)2(2pхCB)2(2рх)2(πz)2(σх)1
NО2 парамагнитна, так как содержит один неспаренный электрон.
в) Молекула N2О3. На МО молекулы оксида азота (III) должны разместиться 28 электронов: по пять азота – 2s22p3 (10 от двух атомов) и по шесть кислорода – 2s22p4 (18 от трех атомов). Если для рассуждения учитывать только 2р-валентные орбитали и их электроны двух атомов азота и трех атомов кислорода, то получим 18 электронов. Учитывая, что в каждой МО может разместиться только 2 электрона, то получим, что все 18 электронов разместятся на 9 МО. N2О3 диамагнитна, так как не содержит неспаренных электронов.
г) Молекула N2O4. На МО молекулы N2O4 должны разместиться 34 электрона: по пять азота – 2s22p3 (10 от двух атомов) и по шесть кислорода – 2s22p4 (24 от четырех атомов). Если для рассуждения учитывать только 2р-валентные орбитали и их электроны двух атомов азота и четырех атомов кислорода, то получим 22 электрона.
Таким образом, молекула N2O4 содержит по два электрона на не связывающих и связывающих МО, значит она диамагнитна.
д) Молекула N2O5. На МО молекулы N2O5 должны разместиться 40 электрона: по пять азота – 2s22p3 (10 от двух атомов) и по шесть кислорода – 2s22p4 (30 от пяти атомов).
26 валентных р-электронов и 14 валентных s-,электронов, участвующих в образовании N2O5 попарно будут находиться на МО, значит она .
е) Молекула N2O. На МО молекулы N2O должны разместиться 16 электрона: по пять азота – 2s22p3 (10 от двух атомов) и шесть кислорода – 2s22p4. 10 валентных р-электронов и 6 валентных s-,электронов, участвующих в образовании N2O попарно будут находиться на не связывающих и связывающих МО, значит она .
Ответ: а, б.
Задача 935.
Какие из перечисленных соединений могут присоединять хлор: a) NО2; б) NН3; в) NО; г) NH2OH? Потому что: 1) хлор — окислитель; 2) у азота есть неподеленная пара электронов; 3) молекула парамагнитна, а азот четырехковалентен; 4) молекула парамагнитна, а ковалентность азота меньше четырех; 5) молекула диамагнитна, а ковалентность азота меньше четырех.
Решение:
a) NО2. На МО молекулы оксида азота (IV) должны разместиться 17 электронов: пять азота – 2s22p3 и по шесть кислорода – 2s22p4 от двух атомов. Размещая их на МО получаем следующую конфигурацию основного состояния:
NО2 [КК(σs)2(σs)2(σsСВ)2(σZСВ)2(πyCB)2(2pхCB)2(2рх)2(πZ)2(σх)1
NО2 парамагнитна, так как содержит один неспаренный электрон.
Молекула NО2 образована связями за счет двух неспаренных электронов атома азота и двух неспаренных электронов одного атома кислорода, а связь азота со вторым атомом кислорода осуществляется за счет свободной электронной пары атома азота и свободной орбитали атома кислорода. Электронное строение молекулы NО2 рассматривается как резонансный гибрид двух форм с изогнутой структурой:
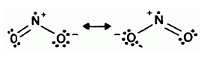
Атом азота в диоксиде азота четырехковалентен.
Таким образом, NO2 не может реагировать с Cl2, хотя молекула , но ковалентность азота меньше четырех.
б) NН3. Три неспаренных p-электрона атома азота участвуют в образовании полярных ковалентных связей с 1s-электронами трёх атомов водорода (связи N—H), четвёртая пара внешних электронов является неподелённой, поэтому аммиак может образовать ковалентную связь по , а с атомом хлора связь не образуется, так как в основном состоянии он имеет неспаренный электрон.
в) NО. Степень окисления азота равна +2, поэтому азот может повышать свою степень окисления, т.е. проявлять свойства восстановителя. В образовании молекулы NO участвуют два неспаренных электрона атома азота с двумя неспаренными электронами атома кислорода, а третий неспаренный электрон азота остается свободным. атома азота равна 2. NO парамагнитна, так как содержит один неспаренный электрон.
Таким образом, NO способна образовывать химическую связь. Так как ковалентность атома азота меньше четырех, то NO способна образовывать химическую связь с атомами, у которых есть неспаренные электроны.
Для NO характерны реакции присоединения галогенов с образованием нитрозилгалогенидов, в этой реакции NO проявляет свойства восстановителя с образованием нитрозилхлорида:
2NО + Cl2 ↔ 2NOCl.
г) NH2OH. Гидроксиламин проявляет свойства восстановителя, при действии на него окислителей выделяются N2 или N2O:
NH2OH + Cl2 + 2ROH ↔ N2↑+ 2KCl + 4H2O.
Ответ: в4, г1).

