Как определяется степень гидролиза изомолярного раствора соли
Задача 1105.
Каково соотношение степеней гидролиза для изомолярных растворов СrCl2 (h1) и СгСI3 (h2): а) h1 > h2; 6) h1 = h2; в) h1 < h2?
Решение:
ПР[Сr(ОН)2] = 2 . 10-20;
КД[Сr(ОН)3] = 1,02 . 10-10.
а) Рассчитаем растворимость Сr(ОН)2:
ПР[Сr(ОН)2] = [Cr2+] . [OH–] = S . (2S)2 = 4S3;
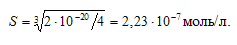
будет определяться растворимостью образовавшегося Сr(ОН)2 и определяется по формуле:
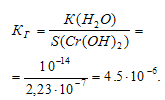
определяется по формуле:
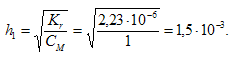
б) определяется константой диссоциации образовавшегося основания Сr(ОН)3 и определяется по формуле:
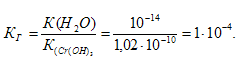
определяется по формуле:
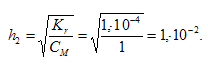
Таким образом, h1 < h2.
Ответ: в.
Как можно уменьшить степень гидролиза соли
Задача 1106.
Как уменьшить степень гидролиза SnCl2: а) нагреть раствор; б) добавить кислоту; в) уменьшить рН раствора?
Решение:
SnCl2 – соль слабого основания [(Sn(OH)2] и сильной кислоты (HCl), поэтому гидролизуется по катиону. С учетом того, что гидролиз в основном протекает по первой ступени, уравнение можно представить уравнением:
Sn2+ + H2O - Sn(OH)+ + H+
Следовательно, раствор соли SnCl2 имеет кислую реакцию среды (рН < 7), так как при гидролизе соли появляется избыток ионов Н+.
а) Диссоциация воды есть процесс эндотермический, то есть сопровождается поглощением тепла: Н2О = Н+ + ОН– – 55,835 кДж/моль. Следовательно по принципу Ле-Шателье, повышение температуры благоприятствует процессу диссоциации воды, то есть с повышением температуры концентрация ионов Н+ и ОН– возрастает, а следовательно, возрастает величина ионного произведения воды. Если нагреть раствор SnCl2, то равновесие сместится вправо, т.е. усилится .
б) При добавлении кислоты в растворе SnCl2 увеличится содержание ионов Н+, что будет подавлять гидролиз, смещая равновесие влево.
в) По принципу Ле-Шателье уменьшение концентрации ионов водорода при уменьшении его рН сместит равновесие влево, т.е. уменьшит . Чтобы усилить , нужно увеличить рН раствора, т.е. нужно добавить сильную щелочь, связывающую ионы водорода.
Ответ: б), в).

