Химические свойства алканов на примере 2-метилбутана
Задача 122.
1. Напишите формулы и дайте названия всем изомерам состава С7Н16.
2. Напишите формулу 2-метил-3-этилгептан и двух его гомологов.
3. Получите бутан всеми возможными способами.
4. Напишите химические реакции характерные для алканов на примере 2-метилбутана.
Решение:
1-е задание. Изомеры гептана
1) CH3-CH2-CH2-CH2-CH2-CH2-CH3 - н-гептан;
2) H3C–CH(CH3)–CH2–CH2–CH2–CH3 - 2-метилгексан;
3) СH3-CH2-CH(CH3)-CH2-CH2-CH3 - 3-метилгексан;
4) H3C–C(CH3)2–CH2–CH2–CH3 - 2,2-диметилпентан;
5) H3C–CH(CH3) – CH(CH3) – CH2–CH3 - 2,3-диметилпентан;
6) H3C–CH(CH3)–CH2–CH(CH3)–CH3 - 2,4-диметилпентан;
7) H3C–CH2–C(CH3)2–CH2–CH3 - 3,3-диметилпентан;
9) H3C - C(CH3)2 –CH(CH3)–CH3 - 2,2,3-метилбутан.
2-е задание. Гомологи 2-метил-3-этилгептана
H3C–CH(CH3)–CH(С2Н5)–CH2–CH2–CH2–CH3 - 2-метил-3-этилгептан
- это химические соединения, имеющие структурную формулу одного типа, например: алканы, алкены, алкины, и т. д. 2-метил-3-этилгептан (изомер декана) относится к гомологическому ряду алканов : метан, этан, пропан, бутан, пентан, гексан, гептан, октан, нонан, декан - это только первые десять, они газы.
Примеры гомологов:
1) CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH3 - н-октан
2) H3C–CH2–CH(C2H5)–CH2–CH2–CH2–CH3 - 3-этилгептан
3-е задание. Получение бутана
1.
CH3-CH2I- + 2Na + I-CH2-CH3 ⇒ CH3-CH2-CH2-CH3 + 2NaI
2. Гидрирование бутина.
Первоначально 1-бутин гидрируют до 1-бутена, а затем 1-бутен вторично гидрируют до бутана:
CH3-CH2-C СН ⇒ CH3-CH2-CH=CH2 ⇒ CH3-CH2-CH2-CH3 (Гидрирование по H2)
СН ⇒ CH3-CH2-CH=CH2 ⇒ CH3-CH2-CH2-CH3 (Гидрирование по H2)
или
СН3-СН2-СН=СН2 + Н2 ⇒ CH3-CH2-CH2-CH3,
СН3—СН2-C СН + 2Н2 ⇒ CH3-CH2-CH2-CH3
СН + 2Н2 ⇒ CH3-CH2-CH2-CH3
3. Дегидратация бутилового спирта
Дегидратацию бутилового спирта проводят в присутствии Al2O3 при температуре 300-400оC:
CH3-CH2-CH2-CH2-OH ⇒ CH3-CH2-CH=CH2 + Н2О;
Затем, полученный 1-бутен гидрируют по водородному радикалу до бутана:
CH3-CH2-CH=CH2 + Н2 ⇒ CH3-CH2-CH2-CH3
4. Получение из солей карбоновых кислот (реакция Дюма)
При сплавлении безводных солей карбоновых кислот с щелочами получаются алканы, содержащие на один атом углерода меньше по сравнению с углеродной цепью исходных карбоновых кислот:
CH3-CH2-CH2-COONa + NaOH ⇒ CH3-CH2-CH2-CH3 + Na2CO3.
5. Метод Фишера-Тропша
Смесь угарного газа и водорода (синтез-газ) пропускают над катализатором при нагревании, получают:
4CO + 9H2 ⇒ C4H10 + 4H2O
6. Реакция Гриньяра
CH3-CH2-CH2-CH2Cl + Mg ⇒ CH3-CH2-CH2-CH2MgCl;
CH3-CH2-CH2-CH2MgCl + H2O ⇒ CH3-CH2-CH2-CH3 + Mg(OH)Cl
7. Электролиз соли (реакция Кольбе)
CH3-CH2-CH2-COONa + 2Н2О электролиз  CH3-CH2-CH2-CH3 + 2СО2↑ + 2Н2↑ + 2NaOH
CH3-CH2-CH2-CH3 + 2СО2↑ + 2Н2↑ + 2NaOH
на аноде на катоде
8. Получение бутана из спирта
Катализатором служит LiAlH4:
CH3-CH2-CH2-CH2ОН ⇒ CH3-CH2-CH2-CH3 + Н2О
4-е задание. Химические реакции характерные для алканов на примере
2-метилбутана.
1) Галогенирование (замещение атома водорода атомом галогена — F, Cl, Br с образованием галогеналкана):
H3C–CH(CH3)–CH2–CH3 + Br2 ⇒ H3C–CBr(CH3)–CH2–CH3 + HBr
2) Сульфирование (замещение атомов водорода сульфогруппой SO3Н с образованием алкансульфокислот RSO3Н). Сульфирующий реагент – серная кислота Н2SO4 (НО-SO3Н).
1. Сульфирование алканов происходит при действии очень концентрированной Н2SO4 при небольшом нагревании. Наиболее легко замещается атом водорода у третичного атомауглерода:
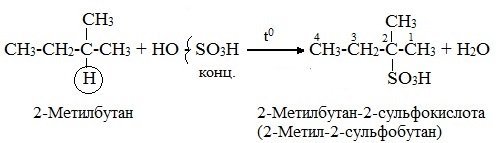
2.При совместном действии сернистого ангидрида и кислорода воздуха под влиянием ультрафиолетовых лучей или добавок перекисей парафиновые углеводороды, даже нормального строения, реагируют с образованием сульфокислот (реакция сульфоокисления):
2H3C–CH(CH3)–CH2–CH3 + 2SO2 + O2 ⇒ 2H3C–C(SO3H)(CH3)–CH2–CH3
2-метил-2-сульфобутан
3. Реакция сульфохлорирования
При совместном действии сернистого ангидрида и хлора при освещении ультрафиолетовым излучением или под влиянием некоторых катализаторов происходит замещение атома водорода с образованием так называемых сульфохлоридов (реакция сульфохлорирования):
2H3C–CH(CH3)–CH2–CH3 + 2SO2 + Cl2 ⇒ 2H3C–C(SO2Cl)(CH3)–CH2–CH3 + HCl
2-метил-2-сульфохлоридбутан
3) Нитрование (замещение атома водорода нитрогруппой – NO2 с образованием нитроалканов R-NO2).
Разбавленная азотная кислота HNO3 (НО-NО2) является нитрующим компонентом. Нитрование алкенов при нагревании называется реакцией М.И.Коновалова. Наиболее легко замещаются атомы водорода у третичного атома:
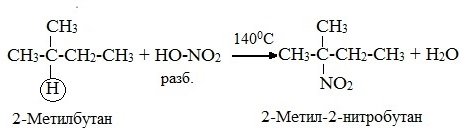
4) Реакции окисления
У 2-метилбутана первичные атомы углерода имеют стпень окисления (-3), вторичный атом углерода имеет степень окисления (-2), а третичный - (-1). При обычных условиях алканы устойчивы к действию сильных окислителей (КМnO4, К2Сr2О7). Алканы могут окисляться с образованием различных соединений:
а) Горение (окисление кислородом воздуха при высоких температурах):
H3C–CH(CH3)–CH2–CH3 + 8О2 ⇒ 5СО2 + 6Н2О
б) Каталитическое окисление алканов
Каталитическое окисление может протекать с разрывом связей С–С и С–Н. Например, при неполном окислении 2-метилбутана происходит разрыв связи (С2–С3) и получается молекула кислоты и ацетона:
H3C–CH(CH3)–CH2–CH3 + 2О2 = 3НC–C(О)–(СН3) + СН3–СООН + Н2О
ацетон уксусная кислота
или
H3C–CH(CH3)–CH2–CH3 + 2О2 ⇒ H3C–CH(CH3)–CH2–СООH + Н2О
Из алканов под влиянием каталитических веществ и нагревании до 200 °C получаются молекулы спирта, альдегида или карбоновой кислоты.
Примеры с 2-метилбутаном:
CH3-CH2-CH(СН3)-CH3 + О2 = CH3-CH2-CH(СН3)-CH2-0Н; (образуется 2-метилбутанол)
CH3-CH2-CH(СН3)-CH3 + О2 = CH3-CH2-CH(СН3)-CО + Н2О (образуется 2-метилбутаналь);
2CH3-CH2-CH(СН3)-CH3 +3О2 = 2CH3-CH2-CH(СН3)-CООН + 2Н2О; (образуется 2-метилбутановая кислота).
Окисление с образованием гидропероксидов:
H3С-CH2-CH(СН3)-CH3 + О2 = CH3-CH2-CH(СН3)-CH2-О-О-Н:
гидропероксид
5) Крекинг (анг. сracking — расщепление) алканов:
а) Термический крекинг — это разрыв связей С - С в молекулах алканов:
H3C–CH(CH3)–CH2–CH3 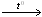 H3C–CH2–CH3 + CH2=CH2.
H3C–CH2–CH3 + CH2=CH2.
б) Термический крекинг в присутствии катализаторов
Термический крекинг проводят в присутствии катализаторов (обычно оксидов алюминия и кремния) при температуре 5000С и атмосферном давлении.Изоалканы термически менее устойчивы, чем алканы нормального строения. Для разветвленных углеводородов преимущественно происходит разрыв связи у третичного или четвертичного атома углерода. При этом с разрывом молекул происходит реакция изомеризации и дегидрирования:
H3C–CH(CH3)–CH2–CH3 ⇒H3C–C(CH3)=CH2 + СН4.
7) Реакции отщепления
а) Дегидрирование
Дегидрирование [отщепление водорода; происходит в результате разрыва связей С - Н; осуществляется в присутствии катализатора (Pt, Pd, Ni, А12О3, Сг2О3) при повышенных температурах (400 — 600°С)]. При этом от молекулы алкена отщепляется молекула водорода:
H3C–CH(CH3)–CH2–CH3 ⇒ H3C–C(CH3)=CH–CH3 + Н2
2-метилбутен-2
8) Пиролиз
Процесс протекает при температуре 1000°С и выше разрываются все связи, образуютс конечные продукты – С и Н2:
H3C–CH(CH3)–CH2–CH3 ⇒ 5С + 6Н2
8) Изомеризация алканов
Алканы нормального строения под влиянием катализаторов и при нагревании способны превращаться в разветвленные алканы без изменения состава молекул, т.е. вступать в реакции изомеpизации. В этих pеакциях участвуют алканы, молекулы которых содержат не менее 4-х углеродных атомов. Например, изомеризация н-пентана в изопентан (2-метилбутан) происходит при 100°С в присутствии катализатора хлорида алюминия:
H3C–(CH2)3–CH3 ⇒ H3C–CН(CH3)–CH2–CH3
н-пентан 2-метилбутан
Теоретически можно предположить, что из 2-метилбутана можно получить 2,2-диметилпропан:
H3C–CН(CH3)–CH2–CH3 = H3C–C(CH3)2–CH3
2-метилбутан 2,2-диметилпропан

